薬剤「経済」学そして「費用」対効果という言葉からは、どうしてもお金のイメージが強くにじむ。では、費用対効果の観点からは、ソバルディやオプジーボ、レパーサは問答無用で「高いからダメ」となるだろうか? 薬剤経済学者はお金だけを考えて新薬を否定する守銭奴だろうか?
決してそんなことはない。薬剤経済学者も、高くてよく効く薬を一律に否定はしない。仮に高額だとしても、それに見合った効果があるのならば、費用対効果の観点からも薬は許容される。「効果」とは、まさに薬の「効き目」である。効き目のものさしになるものを、薬剤経済学では健康アウトカム (Health Outcome)とよぶ。
くすりの効き目を評価できるものさしならば、「血圧」「心筋梗塞発症」「肝がん発症」「平均余命」「死亡数」など、どんなものでも健康アウトカムとなる。以降では、健康アウトカムを単にアウトカムと表記する。
くすりの価値を正しく評価するためには、例えばソバルディであれば
- 医薬品の導入に必要なコスト(介入のコスト。ソバルディのコスト)
- 介入によって、将来削減しうる医療費などのコスト (ソバルディによって削減できる、慢性肝炎、肝硬変や肝がんの治療コスト)
- 介入の導入によるアウトカムの改善度合い (ソバルディで得られる健康上のメリット全般。肝不全死亡の減少や、生命予後の改善など)
以上の3点を定量的に見積もる必要がある。
i. とii. の大小比較は単なる費用比較であって、費用対効果評価とはいえない。i. の介入の費用よりも、ii. の将来的に減らせる医療費が大きくなる(結果的に費用削減となる)ことは、極めてまれである。
i. による医療費増加幅がii. による医療費削減幅を上回って、結果的に医療費が増えたとしても、増えた分に見合った効き目の改善があれば、薬剤経済的にも妥当とされる。「費用対効果に優れる」と「医療費が安くなる」は全く別物なのである。
図1と
図2に、単純化した薬剤経済評価の概念図を示した。今までのくすりを使うと1人あたり2万円 (100人あたり200万円)で、100人中85人を救命できる。一方で新しいくすりを使うと、1人あたり10万円 (100人で1,000万円)で、100人中90人を救える。
「費用対効果」ということばからすぐに連想されるのは、既存薬と新薬、それぞれの費用を効果で割り算することだろう。この数値は
図2左隅の原点から延びた2本の直線の傾きに相当する。直線の傾きは既存薬なら200万円÷85人=2.4万円/1人救命、新薬は1000万÷90人=11.1万円/1人救命となる。この値を費用効果比 (Cost-Effectiveness Ratio: CER)と呼ぶが、CERを比較しても正しい評価はできない。
正しくは、費用も効果も既存薬(コントロール)との差をとって比較する。図中、「既存薬の効果」と「既存薬のコスト」から延びる太線の傾きに相当する。具体的には、コストの差分を効果の差分で割り算して、 (1000万-200万)÷(90人-85人)=160万円/1人救命増加となる。この値を増分費用効果比 (Incremental Cost-Effectiveness Ratio: ICER) と呼ぶ。太線の傾きがICERとなる。経済評価の際には、CERでなくICERで評価するのが基本になる。
卑近なたとえになるが、あるレストランで「1,000円のランチ」と「1,500円のランチ」の2つから選んで注文する際に、考えるのは「それぞれのランチの1円あたり・1calあたりの値段」などではなく、「1,500円ランチと1,000円ランチの質や量の差が、差額の500円に見合っているか?」であろう。くすりの場合もこれと同様に、「コストの差分に見合った効果の改善があるか否か?」を評価するのである。
ICERの値が小さければ、より少ない費用負担で同じ量のアウトカム改善を達成できることになる。すなわち、ICERの値は小さければ小さいほど、「費用対効果に優れる」ことになる。ただし、50万円/1人救命増加と100万円/生存年数1年増加など、異なるアウトカム指標どうしの大小比較はできない。
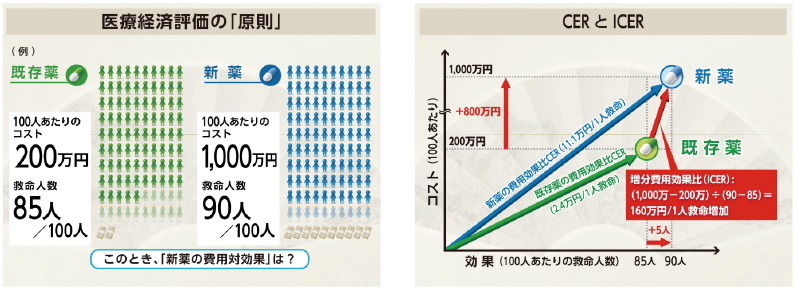 (左)図1 (右)図2
(左)図1 (右)図2